Mở đầu SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 30): Nitrogen tạo ra những hợp chất nào với oxygen? Chúng được tạo thành từ đâu và có những tính chất gì?
Trả lời:
- Nitrogen tạo ra những hợp chất với oxygen là NO, NO2, N2O, N2O3, N2O5,...
- Ở nhiệt độ khoảng 3000oC (hoặc nhiệt độ của lò hồ quang điện), Nitrogen kết hợp trực tiếp với oxygen, tạo ra khí nitrogen monoxide NO.
- Ở điều kiện thường, khí NO không màu kết hợp ngay với oxygen của không khí, tạo ra khí nitrogen dioxide NO2 màu nâu đỏ.
- Ngoài các oxide trên, còn có các oxide khác của nitơ như N2O, N2O3, N2O5, chúng không điều chế được bằng tác dụng trực tiếp giữa nitrogen và oxygen.
- Các oxide của Nitrogen là chất khí và có các tính chất hoá học khác nhau
1. Các oxide của nitrogen - hiện tượng mưa acid
a. Nguồn gốc của các oxide của nitrogen trong không khí
Câu hỏi 1 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 30): Hãy tìm hiểu và cho biết hiện tượng nào trong tự nhiên và quá trình nào trong đời sống của con người là nguồn tạo ra các khí NO, NO2 trong không khí.
Trả lời:
Nguồn tạo ra khí NO, NO2 trong không khí:
+ Trong tự nhiên: Hiện tượng sấm sét.
+ Trong đời sống: Hoạt động của các phương tiện giao thông vận tải, nhà máy nhiệt điện, luyện kim, đốt nhiên liệu …
b. Hiện tượng mưa acid
Câu hỏi 2 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 31): Quan sát Hình 5.2, mô tả quá trình hình thành mưa acid
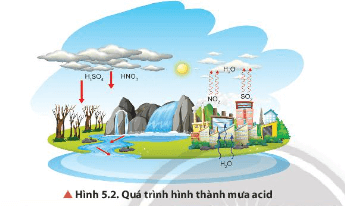
Trả lời:
- Trong thành phần các chất đốt tự nhiên như than đá và dầu mỏ có chứa một lượng lớn lưu huỳnh, còn trong không khí lại chứa nhiều nitrogen. Do hoạt động của núi lửa, cháy rừng, sấm sét hoặc do con người tiêu thụ nhiều nguyên liệu tự nhiên như than đá, dầu mỏ,...tạo thành các oxide của nitrogen (NOx) và sulfur dioxide (SO2) trong khí quyển. Các khí này bị oxi hóa với xúc tác là các ion kim loại trong khói bụi,…và bị hòa tan trong nước tạo thành dung dịch acid HNO3 và H2SO4 gây ra mưa acid.
Câu hỏi 3 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 31): Viết các phương trình hoá học của chuỗi phản ứng tạo ra nitric acid từ nitrogen trong không khí:
N2 → NO → NO2 → HNO3
Trả lời:
Các phương trình hoá học minh hoạ chuỗi phản ứng:
N2(g) + O2(g) ⇌𝑡° 2NO(g)
2NO(g) + O2(g) → 2NO2(g)
4NO2(g) + 2H2O(l) + O2(g) → 4HNO3(aq).
Câu hỏi 4 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 31): Quan sát hình 5.3, hãy nêu một số tác hại của mưa acid

Trả lời:
- Quan sát hình 5.3, Một số tác hại của mưa acid là
+ Làm xói mòn bề mặt các công trình kiến trúc.
+ Ảnh hưởng lớn đến cây trồng.
+ Ảnh hưởng xấu đến các loài sinh vật,...
2. Nitric acid
a. Cấu tạo phân tử, tính chất vật lí của nitric acid
Câu hỏi 5 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 31): Quan sát Hình 5.4a, cho biết các liên kết hoá học giữa các nguyên tử trong phân tử HNO3 thuộc loại liên kết gì. Xác định số oxi hoá của nitrogen trong HNO3. Dự đoán vai trò của HNO3 trong các phản ứng oxi hoá — khử.
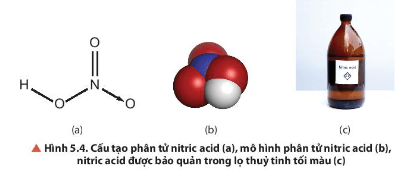
Trả lời:
- Liên kết hoá học giữa các nguyên tử trong phân tử HNO3 là liên kết cộng hóa trị và liên kết cho nhận.
- Số oxi hóa của N trong HNO3 là +5. Đây là số oxi hóa cao nhất của N, do đó trong các phản ứng oxi hóa – khử, HNO3 là chất oxi hóa.
Câu hỏi 6 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 32): Tại sao phải bảo quản nitric acid trong các lọ tối màu?
- Nitric acid tinh khiết kém bền, bị phân huỷ một phần giải phóng khí nitrogen dioxide (NO2) ngay ở điều kiện thường khi có ánh sáng. Do đó, cần bảo quản nitric acid trong các lọ tối màu.
b. Tính chất hóa học và một số ứng dụng thực tiễn quan trọng của nitric acid
Câu hỏi 7 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 32): Hãy tìm hiểu và cho biết HNO3 được ứng dụng vào những lĩnh vực nào trong đời sống và sản xuất.
Trả lời:
- Ứng dụng HNO3
+ Trong công nghiệp sản xuất vũ khí HNO3 là thành phần quan trọng trong sản xuất thuốc nổ TNT, nitrobenzene,...
+ Trong nông nghiệp: Cùng với NH3, HNO3 là nguyên liệu trong sản xuất phân bón (phân đạm 1 lá, 2 lá, ...).
+ Trong công nghiệp: HNO3 được ứng dụng trong quy trình sản xuất thuốc nhuộm, dệt vải, ...
Luyện tập SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 32): Viết phương trình hoá học của các phản ứng khi cho dung dịch HNO3 tác dụng với CuO, Ca(OH)2, CaCO3. Các phản ứng này có phải phản ứng oxi hoá — khử không? Giải thích.
Lời giải:
Các phương trình hoá học:
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Ca(OH)2 → Ca(NO3)2 + 2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + CO2↑ + H2O.
Các phản ứng này không phải là phản ứng oxi hoá – khử; do không có sự thay đổi số oxi hoá của các nguyên tố trước và sau phản ứng.
3. Hiện tượng phú dưỡng
Câu hỏi 8 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 33): Hãy cho biết dấu hiệu nhận biết hiện tượng phú dưỡng.
Trả lời:
- Dấu hiệu nhận biết ao, hồ có hiện tượng phú dưỡng: xuất hiện dày đặc tảo xanh trong nước; nguồn thuỷ sản trong ao hồ bị suy kiệt; xuất hiện mùi hôi thối khó chịu.
Câu hỏi 9 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 33): Hãy nêu một số phương pháp hạn chế hiện tượng phú dưỡng
Trả lời:
- Các biện pháp hạn chế nguồn thải này được đề xuất như:
+ Xây dựng hầm Biogas xử lý nước thải
+ Tạo điều kiện để nước trong kênh rạch, ao, hồ được lưu thông.
+ Xử lí nước thải trước khi cho chảy vào kênh rạch, ao, hồ.
+ Sử dụng phân bón đúng liều lượng, đúng cách, đúng thời điểm trong năm để hạn chế sự rửa trôi ion NO3−, PO43− từ nguồn phân bón dư thừa vào kênh rạch, ao, hồ.
Vận dụng SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 33): Nước thải chăn nuôi là một trong những yếu tố gây nên hiện tượng phú dưỡng cho ao, hồ. Hãy giải thích điều này.
Lời giải:
- Nước thải chăn nuôi chứa lượng lớn nitrogen và phosphorus. Nước thải chăn nuôi chưa qua xử lí, xả vào các ao, hồ, làm tăng hàm lượng nguyên tố dinh dưỡng (nitrogen, phosphorus) trong ao, hồ gây nên hiện tượng phú dưỡng.
Bài tập
Bài tập 1 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 34): Trong công nghiệp, người ta sản xuất nitric acid (HNO3) từ ammonia theo sơ đồ chuyển hoá sau:
a) Viết các phương trình hoá học xảy ra.
b) Để điều chế 200 000 tấn nitric acid có nồng độ 60% cần dùng bao nhiêu tấn ammonia? Biết rằng hiệu suất của phản ứng sản xuất nitric acid theo sơ đồ trên là 96,2%.
Lời giải:

Bài tập 2 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 34): Trong thực tế, nhiều nơi nước thải, phân bón hóa học, thuốc trừ sâu chưa qua xử lý được thả trực tiếp vào ao hồ. Trường hợp nào có thể gây ra hiện tượng phú dưỡng. Giải thích.
Lời giải:
- Nước thải chưa qua xử lí là nguồn thải giàu chất hữu cơ nhất, thường đến từ các cơ sở chăn nuôi, nước thải sinh hoạt gia đình,... do chứa lượng lớn nitrogen và phosphorus thúc đẩy quá trình phú dưỡng diễn ra theo tiến trình nhanh nhất.
Bài tập 3 SGK Hóa 11 Chân trời sáng tạo Bài 5 (trang 34): Khí thải có chứa NO2 góp phần gây ra mưa acid và hiện tượng phú dưỡng. Giải thích.
Lời giải:
- Khí thải chứa NO2 tan trong nước và khí oxygen tạo nitric acid theo phương trình hóa học:
4NO2 + O2 + 2H2O → 4HNO3
