Mở đầu: Trong bảng tuần hoàn các nguyên tố hoá học, kim loại chuyển tiếp dãy thứ nhất bao gồm các nguyên tố từ Sc đến Cu. Cấu hình electron của nguyên tử các nguyên tố này có đặc điểm gì? Chúng có những tính chất vật lí và ứng dụng nào?
Lời giải:
- Cấu hình electron của nguyên tử các nguyên tố này có đặc điểm: có electron hoá trị nằm ở phân lớp 3d và 4s.
- Tính chất vật lí: nhiệt độ nóng chảy, nhiệt độ sôi, độ cứng, khối lượng riêng, độ dẫn điện, độ dẫn nhiệt cao.
- Ứng dụng: chúng có ứng dụng trong nhiều lĩnh vực khác nhau
+ Đồng dùng trong sản xuất các thiết bị như: biến thế, cầu dao điện, dây dẫn điện,…
+ Chromium dùng mạ lên các thiết bị để chống mài mòn, chế tạo hợp kim đặc biệt. Scandium, titanium được dùng để chế tạo hợp kim ứng dụng trong hàng không, vũ trụ. Vanadium dùng trong chế tạo thiết bị chịu nhiệt.
+ Sắt, manganese tạo ra hợp kim với độ bền cơ học tốt, dùng trong quốc phòng, công nghiệp, nông nghiệp, đời sống. Sắt, cobalt dùng để chế tạo nam châm điện. Nickel dùng để chế tạo hợp kim sử dụng trong máy móc, thiết bị.
1. Đặc điểm cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất
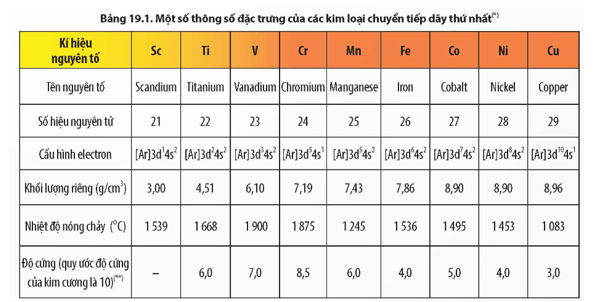
Thảo luận 1: Quan sát Bảng 19.1, hãy cho biết đặc điểm cấu hình electron của các nguyên tử kim loại chuyển tiếp dãy thứ nhất.
Lời giải:
- Cấu hình electron nguyên tử của các nguyên tố kim loại chuyển tiếp dãy thứ nhất có dạng [Ar]3d1÷10 4s1÷2. Nguyên tử của các nguyên tố kim loại chuyển tiếp dãy thứ nhất có electron hoá trị nằm ở phân lớp 3d và 4s.
2. Một số tính chất vật lí và ứng dụng của kim loại chuyển tiếp dãy thứ nhất
Thảo luận 2: Dựa vào số liệu trong Bảng 19.1, Bảng 17.2 và Bảng 18.2, hãy nhận xét, so sánh nhiệt độ nóng chảy, khối lượng riêng, độ cứng của các kim loại chuyển tiếp dãy thứ nhất với kim loại K và Ca. Cho biết độ cứng của Ca là 1,75.
Lời giải:
- Các kim loại chuyển tiếp dãy thứ nhất có nhiệt độ nóng chảy cao hơn, khối lượng riêng lớn hơn, độ cứng lớn hơn các kim loại K, Ca.
Luyện tập: Lấy một số ví dụ về ứng dụng của sắt trong thực tế.
Lời giải:
- Ví dụ về ứng dụng của sắt trong thực tế: Sắt có độ cứng khá cao, dùng để chế tạo hợp kim không gỉ để sản xuất dụng cụ trong y tế.
3. Trạng thái oxi hoá và màu sắc ion của nguyên tố chuyển tiếp
Luyện tập: Hãy viết cấu hình electron của các ion: Cu2+, Fe3+, Cr3+, Mn2+.
Lời giải:

Thảo luận 3: Quan sát Hình 19.1, hãy nhận xét về màu sắc của các ion kim loại chuyển tiếp dãy thứ nhất
Lời giải:
Trong dung dịch, ion của kim loại chuyển tiếp dãy thứ nhất thường có màu.
4. Thí nghiệm
Thảo luận 4: Dự đoán hiện tượng xảy ra trong thí nghiệm xác định hàm lượng muối Fe(II) bằng dung dịch thuốc tím.
Thí nghiệm: Xác định hàm lượng muối Fe(II) bằng dung dịch thuốc tím
Dụng cụ: bộ giá đỡ, bình định mức 100 mL, pipette 10 mL, burette 25 mL, bình tam giác, cốc thuỷ tinh, cân điện tử, thìa thuỷ tinh, quả bóp cao su.
Hoá chất: FeSO4.7H2O rắn, dung dịch KMnO4 0,02 M, dung dịch H2SO4 2 M, nước cất.
Tiến hành:
Bước 1: Cân khoảng 1,5 gam muối FeSO4.7H2O. Cho toàn bộ lượng muối vừa cân vào cốc thuỷ tinh, thêm khoảng 10 mL dung dịch H2SO4, khoảng 40 mL nước cất, khuấy đều cho muối tan hết. Sau đó chuyển dung dịch vào bình định mức 100 mL, dùng nước cất tráng sạch cốc cho tiếp vào bình và định mức đến vạch, lắc đều dung dịch.
Bước 2: Tráng sạch burette bằng nước cất, sau đó tráng lại bằng dung dịch KMnO4. Lắp burette vào giá đỡ, xoay vạch đọc thể tích về phía dễ quan sát. Cho dung dịch KMnO4 vào cốc thuỷ tinh, sau đó rót vào burette (đã khoá) và đưa mức dung dịch về vạch 0.
Bước 3: Dùng pipette lấy 10 ml dung dịch FeSO4 cho vào bình tam giác. Sau đó thêm vào bình khoảng 5 mL dung dịch H2SO4.
Bước 4: Mở khoá burete để nhỏ từ từ từng giọt dung dịch KMnO4 vào bình tam giác đựng dung dịch muối. Liên tục lắc đều bình tam giác. Khi toàn bộ dung dịch ở bình tam giác có màu hồng nhạt ổn định trong khoảng 20 giây thì dừng lại.
Bước 5: Đọc thể tích dung dịch KMnO4 đã sử dụng trên burete.
Bước 6: Lặp lại phép chuẩn độ thêm 2 lần. Lấy giá trị trung bình của 3 lần chuẩn độ.
Lời giải:
- Hiện tượng xảy ra: sau cùng xuất hiện dung dịch màu hồng nhạt.
Thảo luận 5: Từ kết quả chuẩn độ, xác định nồng độ Fe2+ trong dung dịch đã pha.
Lời giải:

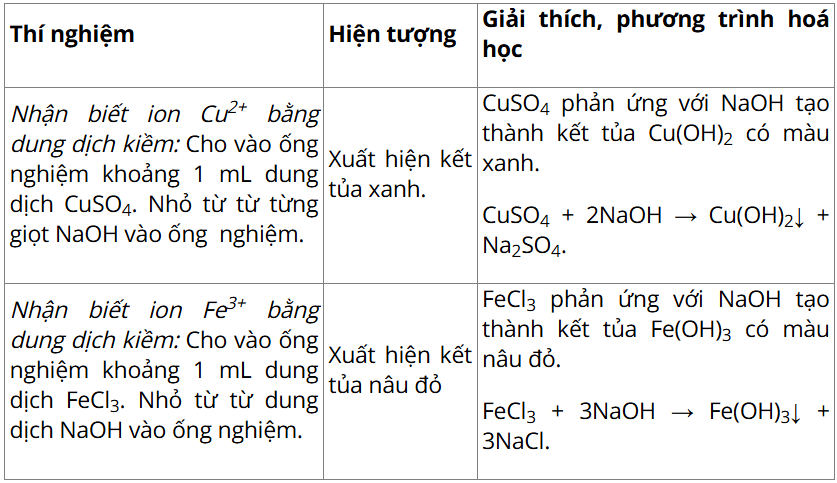
Thảo luận 6: Nêu hiện tượng quan sát được trong thí nghiệm nhận biết các ion Cu2+ và Fe3+, viết phương trình hoá học của phản ứng xảy ra và giải thích.
Lời giải:
Bài tập
Bài tập 1: Viết cấu hình electron của các ion: Cr2+, Fe2+, Ni2+, Co2+, Co3+.
Lời giải:
Cấu hình electron của các ion:
- Cr2+: 1s22s22p63s23p63d4
- Fe2+: 1s22s22p63s23p63d6
- Ni2+: 1s22s22p63s23p63d9
- Co2+: 1s22s22p63s23p63d7
- Co3+: 1s22s22p63s23p63d6
Bài tập 2: Tìm hiểu qua sách, báo hoặc internet, hãy cho biết 5 kim loại có độ dẫn điện và dẫn nhiệt tốt nhất. Qua đó rút ra nhận xét về độ dẫn điện và dẫn nhiệt của các kim loại chuyển tiếp thuộc dãy thứ nhất.
Lời giải:
- Các kim loại có độ dẫn điện, dẫn nhiệt tốt nhất: Ag, Cu, Au, Al, Na.
- Nhận xét: các kim loại chuyển tiếp thuộc dãy thứ nhất có độ dẫn điện và dẫn nhiệt cao.
Bài tập 3: Để xác định hàm lượng của FeCO3 trong quặng siderite, người ta có thể làm như sau: Cân 0,300 g mẫu quặng, xử lí theo một quy trình thích hợp, thu được dung dịch FeSO4 trong môi trường H2SO4 loãng. Coi như dung dịch không chứa tạp chất tác dụng với KMnO4. Chuẩn độ dung dịch thu được bằng dung dịch KMnO4 0,02 M thì dùng hết 12,5 mL. Tính thành phần % theo khối lượng của FeCO3 trong quặng.
Lời giải:
Từ phương trình:
Hoặc bảo toàn electron ta có:
Ta có:
Thành phần % theo khối lượng của FeCO3 trong quặng là: